För omvandlingen av ljusfotoner till elektriska signaler i näthinnan krävs närvaro av det 65-kilodaltons protein som är specifikt för näthinnans pigmentepitel (RPE65). RPE65 finns i näthinnans pigmentepitelceller och konverterar all-trans-retinol till 11-cis-retinol som sedan bildar kromoforen 11-cis-retinal under syncykeln (retinoidcykeln).1
Mutationer av genen RPE65 leder till nedsatt eller obefintlig aktivitet av RPE65 all-trans-retinyl isomeras, vilket blockerar syncykeln och leder till synförlust. Med tiden ackumuleras toxiska ämnen vilket leder till att näthinnans pigmentepitelceller dör och därefter till progressiv fotoreceptorcelldöd.1
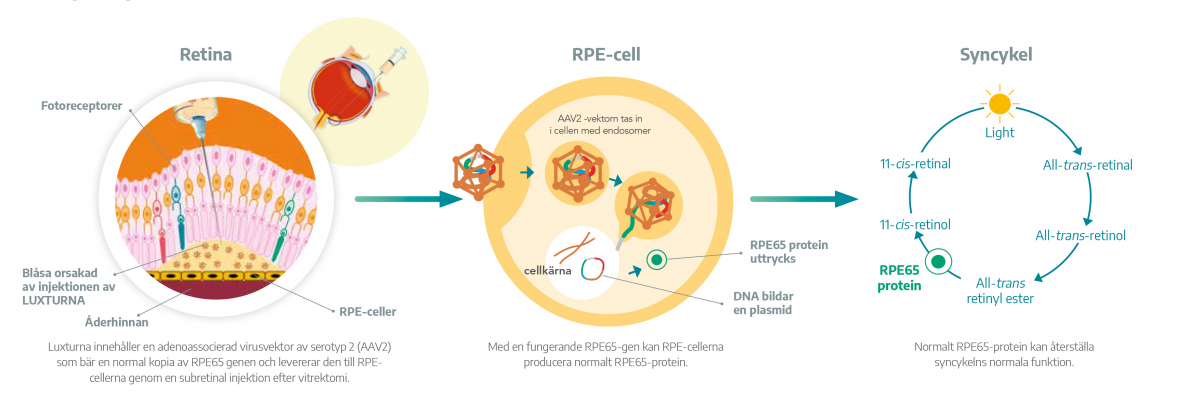
När Luxturna injiceras i det subretinala rummet, sker transduktion av näthinnans pigmentepitelceller med cDNA:t som kodar för normalt humant RPE65 protein (genaugmentationsterapi), vilket gör återställning av syncykeln möjlig.
Referenser
-
Luxturna® SPC
▼Luxturna® (voretigen neparvovek), 5 x 1012 vektorgenom/ml koncentrat och vätska till injektionsvätska, lösning. Rx. Administreras genom subretinal injektion. Voretigen neparvovek är en genöverföringsvektor som utnyttjar kapsiden av en adenoassocierad viral vektor av serotyp 2 (AAV2) för överföring av 65 kDa cDNA av humant retinalt pigmentepitel protein (hRPE65) till näthinnan. Voretigen neparvovek tillverkas av naturligt förekommande AAV med rekombinant DNA-teknik. ATC kod: S01XA. Indikation: Luxturna är avsett för vuxna och barn som har synförlust förorsakad av hereditär retinaldystrofi på grund av bekräftade bialleliska RPE65 mutationer och som har tillräckligt med viabla näthinneceller. Kontraindikationer: Överkänslighet mot den aktiva substansen eller mot något hjälpämne. Okulär eller periokulär infektion. Aktiv intraokulär inflammation. Varningar och försiktighet förknippade med administreringsprocessen: ökat intraokulärt tryck, näthinneperforation, makulära störningar, katarakt, intraokulär inflammation och/eller infektion relaterad till ingreppet, näthinneavlossning och överföring till tredje part. För fullständig information om dosering, administreringssätt, kontraindikationer, varningar och försiktighet, biverkningar samt pris, se www.fass.se . Datum för översyn av produktresumén: 29.04.2024. Vid frågor kontakta Novartis medicinska information via växel 08-732 32 00 eller epost: [email protected] .
Detta läkemedel är föremål för utökad övervakning.
Novartis Sverige AB, Box 1218, 164 28 Kista. www.novartis.se
